Étudier comment la douleur peut jouer un rôle protecteur direct dans l’intestin

Pouvez-vous vous présenter et nous parler de votre parcours, ainsi que de ce qui vous a inspiré pour faire vos dernières recherches ?
Isaac Chiu, Ph.D. – Je suis professeur agrégé à la Harvard Medical School dans le département d’immunologie. J’ai un doctorat. en immunologie à l’Université de Harvard et une formation postdoctorale en neurosciences biologiques de la douleur au Boston Children’s Hospital. Je suis intrigué par la façon dont le système nerveux, le système immunitaire et les microbes s’entremêlent dans la défense de l’hôte, la physiologie et la maladie.
La douleur est une sensation de base, bien que désagréable, qui nous avertit du danger. Il est de plus en plus clair que les nerfs peuvent également avoir d’autres fonctions, notamment envoyer des signaux aux cellules épithéliales qui forment une barrière tissulaire. Nous avons été inspirés pour découvrir si les fibres de la douleur communiquent directement avec les cellules épithéliales intestinales pour les protéger des dommages.
Le Dr Yang et son co-auteur, le Dr Jacobson, ont découvert que la muqueuse de l’intestin était différente lorsque les souris manquaient de fibres douloureuses. Cela a inspiré le travail que nous avons fait dans cette étude. Nous voulions vraiment comprendre comment la douleur régule les niveaux de mucus et si cela a des conséquences sur la protection des tissus intestinaux.
Daping Yang, Ph.D. – Mon doctorat La formation était axée sur l’immunologie et j’ai commencé mon post-doctorat au Chiu Lab il y a trois ans. Je suis très intéressé par la façon dont l’équilibre interne du système de barrière de la muqueuse intestinale est maintenu et comment ce système détecte et s’adapte à l’environnement en constante évolution. Comme nous le savons tous, les patients atteints de maladies inflammatoires ont généralement des douleurs abdominales, que nous avons également observées dans notre modèle de colite in vitro chez le rat. Cependant, on ne sait toujours pas si la douleur, sauf pour avertir d’un danger, est impliquée dans la régulation de la protection de la barrière intestinale.
Crédit d’image : Lightspring / Shutterstock
La présence de la douleur a longtemps été reconnue comme un système d’alerte, nous disant de nous arrêter et de prêter attention à notre corps. Pouvez-vous nous en dire plus sur la douleur elle-même et sur le fonctionnement de cette sonnette d’alarme pour détecter la présence d’un dommage potentiel ?
La douleur fait partie de la réponse du corps à de nombreux stimuli nocifs tels que les blessures thermiques, chimiques ou mécaniques. La douleur est médiée par les neurones récepteurs de la douleur qui contiennent des nerfs situés dans les tissus. Les neurones récepteurs de la douleur expriment de nombreux récepteurs qui leur permettent de reconnaître et de répondre rapidement aux stimuli potentiellement nocifs.
Lorsque la stimulation des neurones récepteurs de la douleur dépasse un certain seuil, elle déclenche un potentiel d’action qui relaie le signal à travers la moelle épinière vers notre cerveau, nous faisant prendre conscience de la douleur et nous avertissant qu’il y a des dommages.
Vos dernières recherches indiquent qu’en plus d’être un système d’alerte, la douleur joue également un rôle protecteur direct dans l’intestin, le protégeant des dommages. Pouvez-vous nous en dire plus sur la manière dont vous avez mené vos études ?
Pour étudier le rôle des neurones récepteurs de la douleur dans la protection de l’intestin et de l’hôte, nous avons élevé des souris dépourvues de ces neurones responsables de la douleur. Puisque la barrière de mucus est la première barrière défensive de la muqueuse intestinale, nous avons d’abord tenté de mesurer l’épaisseur de la couche de mucus en utilisant la coloration par immunofluorescence. Nous avons constaté que l’épaisseur du mucus était significativement réduite par rapport à l’épaisseur du groupe témoin. Avec ces découvertes, nous avons émis l’hypothèse que les neurones récepteurs de la douleur pourraient être impliqués dans la production de mucus. Pour le confirmer, nous avons également utilisé une approche chimique pour activer les neurones récepteurs de la douleur, ce qui a provoqué un épaississement important du mucus.
Nous avons ensuite découvert comment les neurones utilisent un signal appelé CGRP pour communiquer avec les cellules caliciformes, les cellules qui tapissent nos intestins et produisent du mucus. Cela permet aux signaux de douleur d’être directement liés à la sécrétion de mucus. Le microbiote intestinal est un facteur qui amène les neurones à produire du CGRP et stimule les cellules caliciformes à produire du mucus. Nous avons également découvert que la capsaïcine, l’ingrédient des piments présents dans les aliments épicés, stimule également les neurones à produire du CGRP et stimule la production de mucus par les intestins. Enfin, nous avons également constaté que les souris dépourvues de neurones récepteurs de la douleur ou de CGRP étaient plus susceptibles de développer une colite.
Les résultats des souris correspondaient-ils à vos attentes au début de l’étude ? Quels résultats intéressants avez-vous identifiés ?
Nous étions très ouverts sur les attentes au début de notre étude. Nous avons commencé l’étude avec l’hypothèse que la douleur et les neurones impliqués devraient jouer un rôle plus actif dans la régulation du système de barrière intestinale. La découverte la plus intéressante est notre découverte montrant que les cellules caliciformes, cellules productrices de mucus, expriment fortement le récepteur Ramp1, qui reconnaît le neuropeptide CGRP sécrété par les neurones récepteurs de la douleur.
Ces résultats suggèrent que les neurones récepteurs de la douleur peuvent réguler la production de cellules caliciformes par le CGRP qu’ils produisent. Cela signifie également que la production de mucus est étroitement liée au système nerveux. Une autre découverte intéressante est que le microbiome intestinal peut réguler ce processus en stimulant les nerfs pour libérer le CGRP.
Votre recherche a découvert que les cellules caliciformes intestinales sécrètent du mucus protecteur si elles sont stimulées par une interaction directe avec les neurones sensibles à la douleur dans l’intestin. Pouvez-vous nous en dire plus sur les cellules caliciformes concernant vos résultats de recherche ?
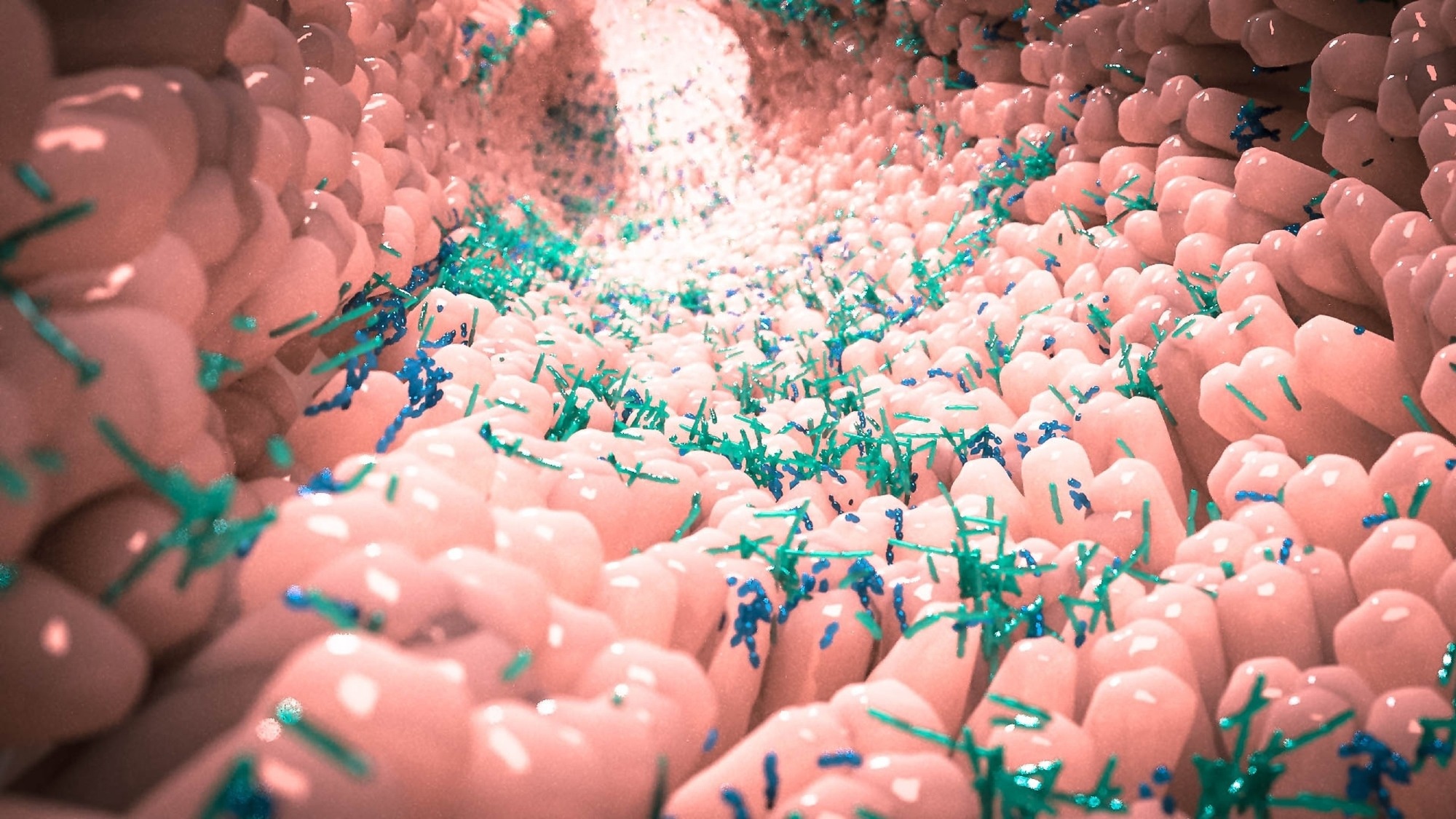
Les cellules caliciformes sont les principaux types de cellules qui produisent et sécrètent du mucus dans l’intestin. Puisque l’intestin est un tissu « muqueux », le mucus est une partie essentielle de l’intestin. D’une part, il recouvre l’intestin et le protège des infections. D’autre part, il maintient un microbiome sain qui peut se nourrir de sucres liés au mucus, ainsi que de mucus gardant une distance entre les microbes nocifs et la paroi intestinale.
Nous avons découvert que les fibres de la douleur peuvent envoyer des signaux directement aux cellules caliciformes pour réguler leur fonction. Chez les souris dépourvues de ces neurones sensibles à la douleur, la muqueuse est plus fine, ce qui conduit à une dysplasie bactérienne, ce qui implique que la communauté microbienne intestinale n’est pas normale. Cela a également rendu les souris plus sensibles à la colite, une inflammation du côlon. Par conséquent, il est important de comprendre comment les cellules caliciformes reçoivent les signaux des neurones et comment cela régule leur survie et leur fonction.
Votre étude a également noté les inconvénients potentiels du soulagement de la douleur. Quels sont ces inconvénients et pourquoi est-il important de considérer les conséquences potentielles de la prévention de la douleur ?
Parce que nous avons découvert que la douleur protège l’intestin en régulant la production de mucus et en maintenant un microbiome sain, si nous supprimons la douleur, cela peut interférer avec cette propriété protectrice. Certaines personnes souffrant de maux de tête et de migraines prennent actuellement des médicaments pour bloquer le CGRP ou son récepteur RAMP1. Nos résultats suggèrent que le blocage de cette voie peut entraîner des problèmes avec la barrière intestinale, y compris la production de mucus et peut-être aussi des problèmes avec le microbiome. On sait déjà que le blocage du CGRP peut entraîner une constipation dans l’intestin.
Plus largement, contrairement aux bloqueurs de CGRP, le blocage des signaux de douleur en général avec des opioïdes ou d’autres médicaments peut avoir des conséquences inattendues sur la fonction de barrière intestinale ou la production de mucus auxquelles il faut faire attention.
Quelles sont les prochaines étapes pour poursuivre votre recherche ?
Nous sommes très intéressés à mieux définir comment les neurones communiquent avec les cellules intestinales. Nous nous intéressons en particulier à la manière dont les fibres de la douleur interagissent avec les cellules immunitaires de l’intestin, ce qui peut avoir des conséquences sur l’inflammation. Une autre question très intéressante consiste à déterminer comment notre microbiome affecte les fibres de la douleur dans l’intestin.
Une implication de notre recherche est que, via ces nerfs, la signalisation du microbiome régule les niveaux de mucus. Par conséquent, l’identification des produits des microbes agissant sur les fibres douloureuses peut être importante.
Où les lecteurs peuvent-ils obtenir plus d’informations ?
Lien vers Chiu Lab : http://chiulab.med.harvard.edu
Lien d’étude: https://www.sciencedirect.com/science/article/pii/S0092867422011965?dgcid=coauthor
A propos des entretiens :
Isaac Chiu, Ph.D. – Isaac Keough est professeur agrégé au Département d’immunologie de la Harvard Medical School. La recherche centrale du Dr Chiu se concentre sur les interactions neuro-immunitaires dans la douleur et la défense de l’hôte
Le Dr Chiu a obtenu son doctorat. Il a obtenu son doctorat en immunologie de la Harvard Medical School dans le laboratoire de Mike Carroll, puis a suivi sa formation postdoctorale en neurobiologie de la douleur dans le laboratoire de Clifford Wolff au Boston Children’s Hospital. Il a commencé son poste de professeur indépendant à la Harvard Medical School en 2014. Le Dr Chiu a reçu le Burroughs Wellcome Fund Investigators Award in Infectious Diseases Pathogenese, le NIH Director’s New Innovator Award et le Chan-Zuckerberg Initiative Ben Barres Award.
Daping Yang, Ph.D. – Daping Yang a obtenu son doctorat. Il s’est spécialisé en immunologie à l’Institut des sciences biologiques de Shanghai en Chine, où il a développé son intérêt pour la recherche. Rejoignez le laboratoire du professeur Isaac Keogh à la Harvard Medical School en tant qu’étudiant postdoctoral en 2020, dans le but de comprendre le rôle de l’axe intestinal dans la protection de la barrière muqueuse intestinale sous l’homéostasie et l’inflammation. Ses travaux actuels portent sur la façon dont la douleur et les nocicepteurs protègent la santé intestinale.